
弗吉尼亚州 COVID- 19更新
十二月29 , 2021
尊敬的同事:
感谢您在应对 COVID- 19疫情过程中给予的持续合作。请访问弗吉尼亚州卫生部 (VDH) 网站,获取当前的临床和公共卫生指导、流行病学数据和其他信息。本函件包含以下主题的更新:
- 更新并缩短普通人群隔离检疫指南
- SARS-CoV- 2感染或暴露的医护人员管理最新指南
- 治疗学更新
更新并缩短普通人群隔离检疫指南
美国疾病控制与预防中心(CDC)更新了针对普通人群的隔离和检疫指南。如果 COVID- 19患者无症状或症状正在消退,则可以在5天后结束隔离。他们应在接下来的5天内继续在与他人接触时佩戴口罩。无论疫苗接种状况如何,这些建议均适用。隔离期从10天缩短,因为目前的证据表明,大多数 SARS- COV 2传播发生在疾病发作前1 - 2天和症状出现后2 - 3天。
CDC 还改变并缩短了针对接触 COVID- 19人员的隔离指导:
- 在过去2月内接受过加强疫苗或完成过强生 (J&J) 初级系列疫苗,或在过去6月内完成过 mRNA 初级系列疫苗的人,在接触过 COVID- 19患者后无需隔离。当与他人接触时,他们应在接触后10天内佩戴口罩。
- 未接种疫苗或超过2个月前完成强生初级系列且未接种加强针的人,或超过6个月前完成 mRNA 初级系列且未接种加强针的人,在接触 COVID- 19患者后,应隔离5天,并继续佩戴口罩5天。如果个人无法进行切实可行的隔离,则必须在接触后佩戴口罩10天。
无论疫苗接种情况如何,那些接触过 COVID- 19患者的人都应在5天接受检测(如果可能)。如果他们出现症状或检测呈阳性,也应立即隔离。
目前,CDC 建议医疗保健患者和疗养院居民遵循 9 月2021隔离和检疫指导。我们预计 CDC 将很快更新针对特定行业的指导。
CDC 更新的隔离指南反映了南非和英国的数据,这些数据表明,接种两剂 mRNA 疫苗后对 Omicron 感染的疫苗有效性约为35 %。经过加强剂量后,疫苗对 Omicron 感染的有效性增加至75 %。请继续鼓励所有16岁及以上的患者在符合条件时接种 COVID- 19加强疫苗,并鼓励所有5岁及以上的人士完成其主要接种系列。
SARS-CoV- 2感染或暴露的医护人员管理最新指南
CDC发布了最新的医护人员隔离和检疫指南(HCP),缩短了他们在感染COVID-19 后的隔离时间。此外,在医护人员严重短缺的情况下,CDC发布了最新的应急和危机管理指南。上文详述的新的普通人群隔离检疫指南不适用于 HCP;医疗机构应针对 HCP 执行以下指南:
包括疗养院在内的医疗机构可能会实施新的CDC 应急和危机情况指导,以在必要时缩短 HCP 的工作限制时间,从而缓解医疗人员短缺。该指南基于目前关于 Omicron 变体的有限信息,并将根据新信息的需要进行更新。即使出现轻微 COVID- 19症状的医护人员也应优先进行病毒检测。确保使用能够检测到 SARS- COV 2测试来执行SARS- COV 2测试,考虑到当前流行的变体。
感染 SARS- COV 2医护人员重返工作岗位:常规情况下,感染SARS- COV 2且无症状或轻微症状且症状好转的医护人员,经检测阴性后, 7天后可返回工作岗位,如遇人员短缺,隔离时间可进一步缩短(见下表)。
- 已接种所有推荐剂量的 COVID- 19疫苗(包括加强剂)的无症状 HCP 在高风险接触后无需在家隔离(有关高风险接触的常规条件下的检测指南,请参阅下表)。
- 尚未接种所有 COVID- 19疫苗剂量(包括加强剂量)的无症状 HCP 可以在之前建议的14天隔离期之前返回工作岗位,前提是他们没有出现症状或 SARS- COV检测呈阳性2 (有关高风险暴露的检测指南,请参阅下表)。
- 接触风险较低的无症状 HCP,无论是否加强接种、接种疫苗或未接种疫苗,都没有工作限制或检测建议。
- 有关暴露类型的更多信息,请参阅CDC 表格中基于疫苗接种状况和暴露类型的 HCP 建议工作限制。
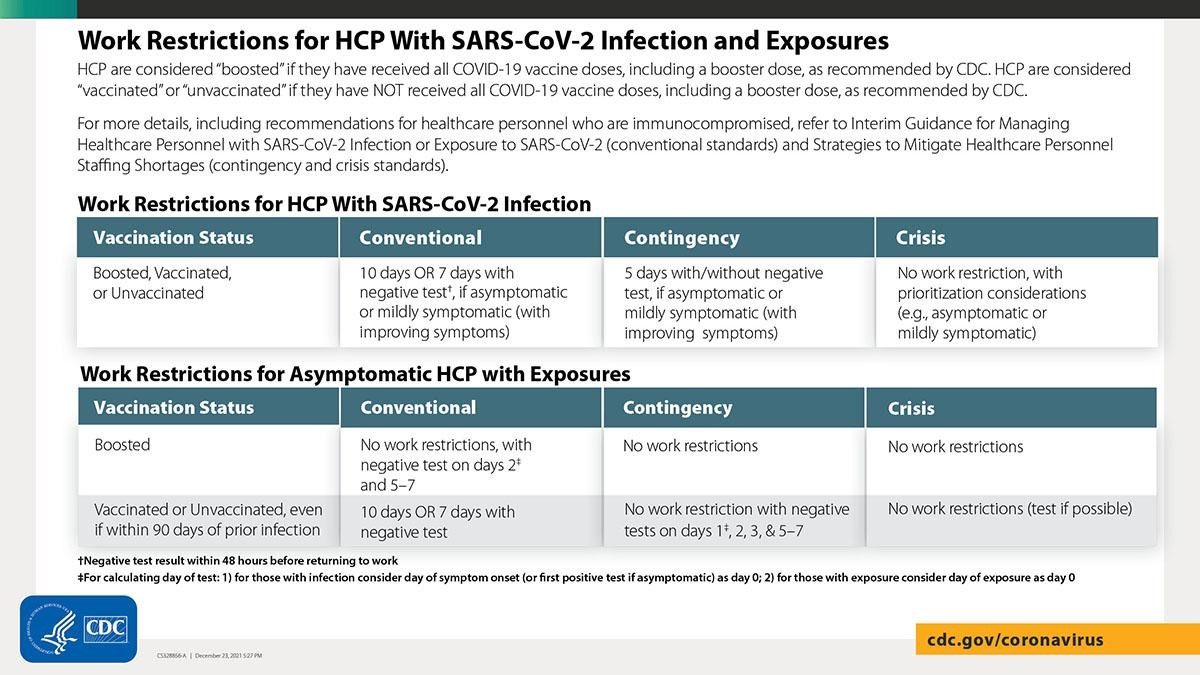
治疗学更新
上周,美国食品药品监督管理局 (FDA) 批准了首批用于治疗 COVID- 19的口服抗病毒药物。
- 辉瑞公司的 Paxlovid 是尼玛瑞韦和利托那韦的组合,被授权用于治疗已确诊为轻度至中度 COVID- 19的成人和儿科门诊患者( 12岁及以上,体重至少40公斤 [ 88磅]),这些患者有发展为重症 COVID- 19高风险。
- 默克公司的莫努皮拉韦被授权用于治疗已确诊为轻度至中度 COVID- 19成年人,这些患者有发展为重症 COVID- 19高风险,并且 FDA 授权的替代 COVID- 19治疗方案无法获得或临床上不适用。
两种治疗均需凭处方获得,并应在确诊 COVID- 19后尽快开始,且在症状出现后5天内开始。从本周开始,Paxlovid 和 molnupiravir 将在联邦的一些药店出售;然而,这两种药物的初始供应量将非常有限。当药房收到这些抗病毒药物时,弗吉尼亚州的地点列表将在治疗学网页上提供。
EVUSHELD (tixagevimab 联合 cilgavimab,阿斯利康)已获得FDA 批准,用于对中度至重度免疫功能低下12岁及以上患者进行 COVID- 19暴露前预防 (PrEP),或因曾对 COVID- 19疫苗或其某一成分产生严重不良反应而医学上不建议接种 COVID- 19疫苗的患者。弗吉尼亚州可供分发的 EVUSHELD 供应量有限;初始供应将提供给现有的单克隆抗体管理站点。
负责防范和应对 (ASPR) 的助理部长计划自 1 月3起、 2022暂停向各州运送 bamlanivimab 和 etesevimab 合用药、etesevimab 单独用药以及 REGEN-COV,等待 CDC 更新数据,因为当前数据显示,bamlanivimab 和 etesevimab 合用(Bam/Ete)或 casirivimab 和 imdevimab(REGEN-COV)不太可能对 Omicron 变体有效。Sotrovimab 似乎保留了对抗 Omicron 变体的活性。FDA 更新了bamlanivimab 和 etesevimab 联合用药、 REGEN-COV和sotrovimab的医疗保健提供者情况说明书,其中包含有关针对 Omicron 变体 (B. 1 . 1 . 529 /BA. 1 ) 的预期活性的具体信息。
再次感谢您在我们应对 COVID- 19疫情期间的持续合作。祝您度过一个安全、快乐的假期。
真挚地,
M. Norman Oliver,医学博士,文学硕士
州卫生专员
