
弗吉尼亚州 COVID- 19更新
八月26 , 2021
尊敬的同事:
感谢您在应对 COVID- 19疫情过程中给予的持续合作。请访问弗吉尼亚州卫生部 (VDH) 网站,获取当前的临床和公共卫生指导、流行病学数据和其他信息。本函件包含以下主题的更新:
- FDA 全面批准辉瑞-BioNTech COVID- 19疫苗
- 针对普通成年人群的 mRNA 疫苗加强剂量将于 9 月中旬开始接种
- 同时接种 COVID- 19和流感疫苗
- 有关呼吸道合胞病毒的更多更新
FDA 全面批准辉瑞-BioNTech COVID- 19疫苗
8 月23日, 2021美国食品药品监督管理局 (FDA) 全面批准了首个 COVID- 19疫苗,即辉瑞-BioNTech COVID- 19疫苗,适用于16岁及以上人群。该疫苗将以 Comirnaty 的名称上市销售。FDA 针对 Comirnaty 的紧急使用授权 (EUA) 将继续覆盖年龄为12至15岁的个人,并向年龄12岁及以上的某些免疫功能低下的个人注射第三剂。FDA 批准的疫苗和 FDA 授权的疫苗具有相同的配方,可以互换使用以提供 COVID- 19疫苗接种系列,而不会出现任何安全性或有效性问题。疫苗的储存、处理和订购流程没有改变。FDA 已更新其Comirnaty 和辉瑞-BioNTech 情况说明书,供管理疫苗的医疗保健提供者以及接种者和护理人员使用。CDC 免疫实践咨询委员会 (ACIP) 将于 8 月30开会讨论针对 Comirnaty 的最新建议。
这项批准是一个重要的里程碑,它可以让任何担心接种疫苗的人放心,COVID- 19疫苗是有效且安全的。根据临床试验结果,Comirnaty 在预防 COVID- 19疾病方面的有效性为91 %。FDA 还对心肌炎和心包炎病例进行了严格的上市后安全监测。现有的短期数据表明,大多数人已经完全康复,但有些患者确实需要重症监护支持。研究发现, 12至17岁男性的风险最高。研究还发现,疫苗接种者的心肌炎风险远低于实际感染 COVID- 19疾病期间和之后的心肌炎风险。
经 FDA 全面批准,Comirnaty 现可用于非紧急情况。尽管 FDA 的完全批准通常允许产品的“非说明书用途”使用,但所有 COVID- 19疫苗的接种仍必须按照 CDC 的 COVID- 19疫苗接种计划要求以及CDC 、 ACIP和FDA的建议进行。这适用于 EUA 和 FDA 批准的 COVID- 19疫苗。不建议超说明书使用任何 COVID- 19疫苗,这可能会使提供者面临以下风险:
- 《PREP 法案》或《PREP 法案》声明可能不涵盖非说明书产品的管理;因此,供应商可能无法免于索赔。
- 接受非说明书剂量治疗的个人在发生不良事件后可能没有资格根据“对策伤害赔偿计划”获得赔偿。
- CDC 已明确规定了 CDC COVID- 19疫苗接种计划的范围,包括如何在该计划中使用美国政府提供的疫苗。提供非说明书剂量药物的提供者将违反 CDC 计划提供者协议,这可能会影响他们继续作为 CDC 计划提供者的能力。
- 付款人可能无法报销管理费。
在 FDA 审查有关 Moderna 和强生疫苗实际使用情况的数据期间,它们将继续通过 EUA 安全接种。
mRNA疫苗加强剂将于9月中旬开始面向普通人群接种
8 月18日, 2021美国卫生与公众服务部 (HHS) 发布了一份联合声明,宣布了政府为已接种完整系列 mRNA 疫苗的普通人群提供 COVID- 19加强剂量的计划。加强剂量是指当对一系列主要疫苗的初始充分免疫反应可能随着时间的推移而减弱时所注射的疫苗剂量。尽管 COVID- 19疫苗继续为预防重症、住院和死亡提供强有力的保护,但最近的证据表明,对某些人群而言,对轻度和中度 COVID- 19疾病的保护会随着时间的推移而降低。人们担心,未来几个月对最坏的 COVID- 19结果的保护可能会减弱,尤其是对于患重病风险较高或在疫苗推出早期阶段接种过疫苗的人群。作为回应,VDH 发布了一份新闻稿,并更新了针对公众和医疗保健提供者的疫苗接种常见问题解答。
根据这些新出现的数据,目前提出的计划是,任何年龄18岁或以上、接种过两剂辉瑞-BioNTech (Comirnaty) 或 Moderna 疫苗的人都应计划在接种第二剂疫苗后至少八个月接种一剂加强剂,接种时间从 9 月20 、 2021那一周开始。这些建议(包括时间表)可能会根据 FDA、ACIP 和 CDC 的审查流程而改变。目前不建议使用助推器。ACIP 于 8 月30举行的会议将讨论加强剂量问题。请关注 CDC 和 VDH 网站以获取最新信息,因为这些信息可能会发生变化;一旦我们有更多信息,我们将立即发送更新。
在美国卫生与公众服务部宣布这一消息时,不建议接种强生疫苗的人接种加强剂量,因为做出此决定所需的临床试验数据尚未公布。8 月25日,强生公司报告称,接种疫苗的个体获得了可持续八个月的强效保护,并且加强剂量可使18 - 55岁人群的刺突结合抗体显著增加,而接受较低加强剂量的人群中, 65岁及以上人群的刺突结合抗体也显著增加。这些数据可能会被 FDA 和 CDC 审查,以提供该产品的加强剂建议。
在准备加强剂量时,我们需要确保有足够的 COVID- 19疫苗提供者来满足需求。如果您还没有,请考虑成为提供商来支持您的社区。欲了解更多信息,请访问 VDH 的提供商注册页面。此外,弗吉尼亚疫苗管理和分配交易所(VaxMax) 为参与的医疗保健提供者提供疫苗订购、管理和分发的资源。如果您之前担心最低订单量太大,弗吉尼亚州现在有一个小批量货物重新分配计划,可以向供应商办公室提供较小数量的货物。请考虑立即注册成为 COVID- 19疫苗提供者。
同时接种 COVID- 19和流感疫苗
随着流感季节的临近,同一天为患者提供 COVID- 19和流感疫苗可能会带来显著的后勤优势。根据C DC 对 COVID- 19疫苗的临床考虑,您可以安全地接种 COVID- 19和流感疫苗(活疫苗、减毒疫苗和非活流感疫苗),而无需考虑时间。这包括同一天接种 COVID- 19和流感疫苗,以及在14天内同时接种。在决定是否同时接种疫苗时,请考虑:
- 患者是否已经或有可能没有接种推荐的疫苗
- 患者罹患疫苗可预防疾病的风险
- 疫苗的反应原性概况
- 避免错过接种疫苗机会的可能性
接种多种疫苗的最佳做法包括:
- 在每个注射器上贴上标签,标明疫苗的名称和剂量(数量)、批号、配制者的姓名首字母以及准确的有效期(如果适用)。
- 如果可能,将注射部位间隔1英寸或更多。
- 如果可能,请在不同的肢体上接种 COVID- 19疫苗和更容易引起局部反应的疫苗(即佐剂流感疫苗)。
流感疫苗接种将减轻流感疾病、住院和死亡对医疗保健系统造成的负担,并有助于节省用于治疗 COVID- 19和其他疾病的医疗资源。
有关呼吸道合胞病毒的更多更新
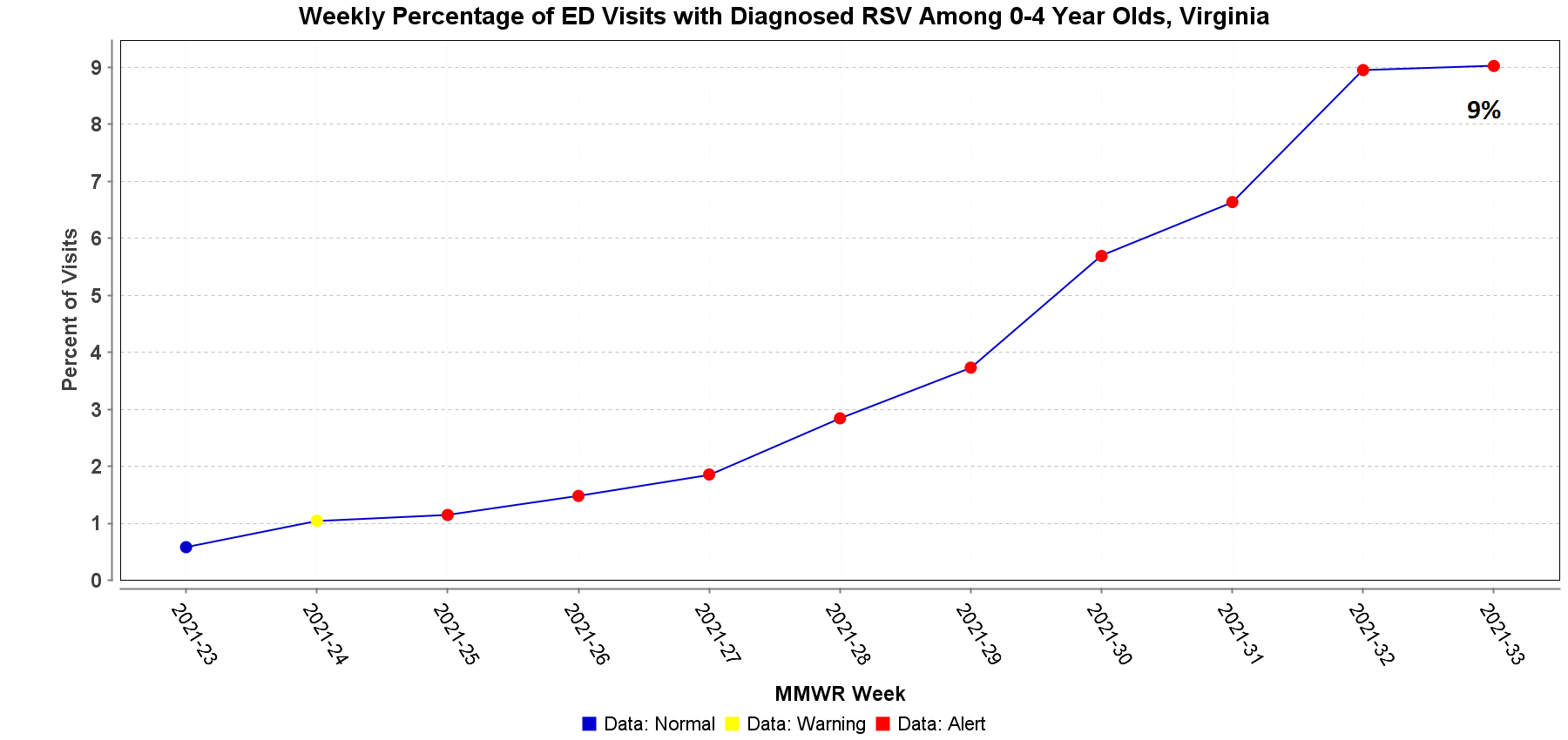
在我们8 月份的6 、 2021致各位同事的信中,我们提供了有关呼吸道合胞病毒 (RSV) 预防的信息。此后,美国儿科学会(AAP)更新了帕利珠单抗预防的临时指南。AAP 强烈支持医疗服务提供者考虑对符合当前资格建议的患者使用帕利珠单抗。修订后的指南更新了帕利珠单抗的给药时间,以适应今年呼吸道合胞病毒季节性的变化。AAP 的建议适用于呼吸道合胞病毒传播率较高的地区,与典型的秋冬季节一致。VDH 报告的 RSV 疫情数量有所增加。迄今为止,已报告的呼吸道合胞病毒疫情在 6 月份发生 1 起,7 月份发生 3 起,8 月份发生 11 起。在 8 月15至21周内,弗吉尼亚州0至4岁儿童急诊就诊中,有9 % 被诊断出患有呼吸道合胞病毒。
与往常一样,我真诚感谢您在这些充满挑战的时期继续与我们合作。如果您对 COVID- 19有任何疑问,请联系您当地的卫生部门。
真挚地,
M. Norman Oliver,医学博士,文学硕士
州卫生专员
